Το Levemir για τη θεραπεία του διαβήτη
Εμπορικό σήμα: Levemir
Γενικό όνομα: ινσουλίνη Detemir
Μορφή δοσολογίας: ένεση
Περιεχόμενα:
Περιγραφή
Κλινική Φαρμακολογία
Κλινικές μελέτες
Ενδείξεις και χρήση
Αντενδείξεις
Προειδοποιήσεις
Προφυλάξεις
Ανεπιθύμητες ενέργειες
Υπερδοσολογία
Δοσολογία και χορήγηση
Πώς παρέχεται
Levemir, ινσουλίνη detemir (προέλευση rDNA), πληροφορίες για τον ασθενή (στην απλή αγγλική γλώσσα)
Περιγραφή
Το Levemir® (έγχυση ινσουλίνης detemir [rDNA προέλευσης]) είναι ένα αποστειρωμένο διάλυμα ινσουλίνης detemir για χρήση ως ένεση. Η ινσουλίνη detemir είναι ένα βασικό ανάλογο ινσουλίνης μακράς δράσης, με διάρκεια δράσης έως 24 ώρες, που παράγεται από α διαδικασία η οποία περιλαμβάνει έκφραση ανασυνδυασμένου DNA σε Saccharomyces cerevisiae ακολουθούμενη από χημική ουσία τροποποίηση.
Η ινσουλίνη detemir διαφέρει από την ανθρώπινη ινσουλίνη κατά το ότι το αμινοξύ θρεονίνης στη θέση Β30 έχει παραλειφθεί και μια αλυσίδα λιπαρού οξέος C14 έχει συνδεθεί με το αμινοξύ Β29. Η ινσουλίνη detemir έχει μοριακό τύπο C267H402O76N64S6 και μοριακό βάρος 5916,9. Έχει την ακόλουθη δομή:
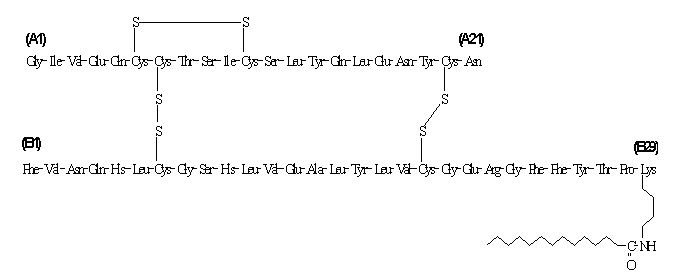
Το Levemir είναι ένα διαυγές, άχρωμο, υδατικό, ουδέτερο στείρο διάλυμα. Κάθε χιλιοστόλιτρο Levemir περιέχει 100 U (14,2 mg / mL) ινσουλίνης detemir. Κάθε χιλιοστόλιτρο φιαλιδίου Levemir 10 mL περιέχει τα αδρανή συστατικά 65,4 mcg ψευδάργυρο, 2,06 mg m-κρεζόλης, 30,0 mg μαννιτόλη, 1,80 mg φαινόλης, 0,89 mg διένυδρου φωσφορικού δινατρίου, 1,17 mg χλωριούχου νατρίου και ύδατος για ένεση. Κάθε χιλιοστόλιτρο φυσιγγίου Levemir 3 mL PenFill®, FlexPen® και InnoLet® περιέχει τα αδρανή συστατικά 65,4 mcg ψευδαργύρου, 2,06 mg m-κρεζόλης, 16,0 mg γλυκερόλης, 1,80 mg φαινόλης, 0,89 mg διένυδρου φωσφορικού δινατρίου, 1,17 mg χλωριούχου νατρίου και ύδατος για ένεση. Μπορεί να προστεθεί υδροχλωρικό οξύ και / ή υδροξείδιο του νατρίου για τη ρύθμιση του ρΗ. Το Levemir έχει ρΗ περίπου 7,4.
μπλουζα
Κλινική Φαρμακολογία
Μηχανισμός δράσης
Η κύρια δραστηριότητα της ινσουλίνης detemir είναι η ρύθμιση του μεταβολισμού της γλυκόζης. Οι ινσουλίνες, συμπεριλαμβανομένης της ινσουλίνης detemir, ασκούν την ειδική δράση τους μέσω της δέσμευσης σε υποδοχείς ινσουλίνης.
Η συνδεδεμένη με υποδοχέα ινσουλίνη μειώνει τη γλυκόζη του αίματος διευκολύνοντας την κυτταρική πρόσληψη γλυκόζης σε σκελετικούς μύες και λίπος και αναστέλλοντας την παραγωγή γλυκόζης από το ήπαρ. Η ινσουλίνη αναστέλλει τη λιπόλυση στα λιποκύτταρα, αναστέλλει την πρωτεόλυση και ενισχύει τη σύνθεση πρωτεϊνών.
Φαρμακοδυναμική
Η ινσουλίνη detemir είναι ένα διαλυτό ανάλογο βασικής ανθρώπινης ινσουλίνης μακράς δράσης με ένα σχετικά επίπεδο προφίλ δράσης. Η μέση διάρκεια δράσης της ινσουλίνης detemir κυμάνθηκε από 5,7 ώρες στη χαμηλότερη δόση έως 23,2 ώρες στην υψηλότερη δόση (περίοδος δειγματοληψίας 24 ώρες).
Η παρατεταμένη δράση του Levemir προκαλείται από την αργή συστηματική απορρόφηση της ινσουλίνης detemir μορίων από τη θέση ένεσης λόγω ισχυρής αυτοσύνδεσης των μορίων φαρμάκου και της αλβουμίνης δεσμευτικός. Η ινσουλίνη detemir κατανέμεται πιο αργά στους περιφερειακούς ιστούς στόχους, καθώς η ινσουλίνη detemir στην κυκλοφορία του αίματος συνδέεται σε μεγάλο βαθμό με την αλβουμίνη.
Το σχήμα 1 δείχνει την ταχύτητα έγχυσης γλυκόζης από μια μελέτη σφιγκτήρα γλυκόζης σε ασθενείς με διαβήτη τύπου 1.
Εικόνα 1: Προφίλ δραστηριότητας σε ασθενείς με σακχαρώδη διαβήτη τύπου 1 σε 24ωρη μελέτη σφιγκτήρων γλυκόζης
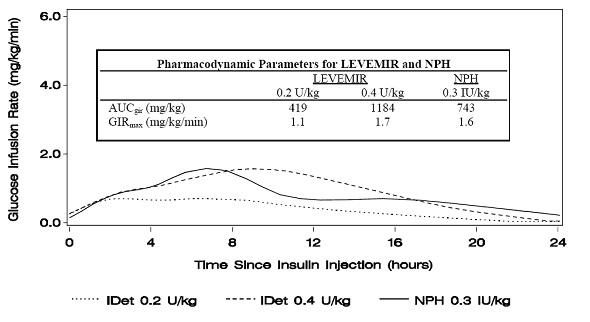
Το σχήμα 2 δείχνει την ταχύτητα έγχυσης γλυκόζης από μια μελέτη σφιγκτήρα γλυκόζης διάρκειας 16 ωρών σε ασθενείς με διαβήτη τύπου 2. Η μελέτη σφιγκτήρα τερματίστηκε στις 16 ώρες σύμφωνα με το πρωτόκολλο.
Εικόνα 2: Προφίλ δραστηριότητας σε ασθενείς με διαβήτη τύπου 2 σε μια μελέτη σφιγκτήρα γλυκόζης διάρκειας 16 ωρών
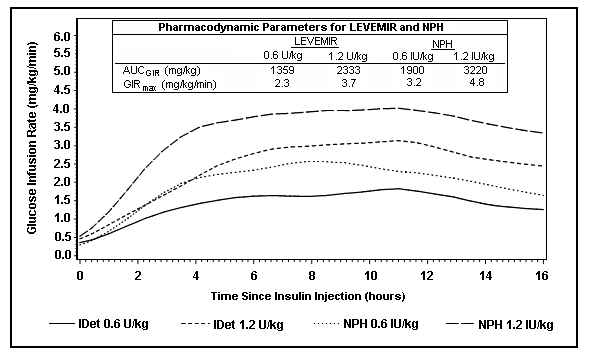
Για τις δόσεις στο διάστημα από 0,2 έως 0,4 U / kg, το Levemir ασκεί περισσότερο από το 50% της μέγιστης δράσης του από 3 έως 4 ώρες έως περίπου 14 ώρες μετά τη χορήγηση της δόσης.
Σε μια μελέτη σφιγκτήρα γλυκόζης, η συνολική γλυκοδυναμική επίδραση (AUCGIR 0-24h) [μέση mg / kg ± SD (CV)] τεσσάρων ξεχωριστών υποδόριες ενέσεις στον μηρό ήταν 1702,6 ± 489 mg / kg (29%) στην ομάδα του Levemir και 1922,8 ± 765 mg / kg (40%). για το NPH. Η κλινική σημασία αυτής της διαφοράς δεν έχει τεκμηριωθεί.
Φαρμακοκινητική
Απορρόφηση
Μετά την υποδόρια ένεση ινσουλίνης detemir σε υγιή άτομα και σε ασθενείς με διαβήτη, ινσουλίνη detemir οι συγκεντρώσεις στον ορό έδειξαν βραδύτερη, πιο παρατεταμένη απορρόφηση σε διάστημα 24 ωρών σε σύγκριση με τον άνθρωπο NPH ινσουλίνη.
Η μέγιστη συγκέντρωση στον ορό (Cmax) επιτυγχάνεται μεταξύ 6 και 8 ωρών μετά τη χορήγηση.
Η απόλυτη βιοδιαθεσιμότητα της ινσουλίνης detemir είναι περίπου 60%.
Διανομή και Εξάλειψη
Περισσότερο από 98% της ινσουλίνης detemir στην κυκλοφορία του αίματος δεσμεύεται με την αλβουμίνη. Το Levemir έχει μικρό φαινόμενο όγκο κατανομής περίπου 0,1 L / kg. Το Levemir, μετά από υποδόρια χορήγηση, έχει τελικό χρόνο ημιζωής 5 έως 7 ώρες ανάλογα με τη δόση.
Ειδικοί πληθυσμοί
Παιδιά και έφηβοι - Οι φαρμακοκινητικές ιδιότητες του Levemir ερευνήθηκαν σε παιδιά (6 έως 12 ετών) και σε εφήβους (13 έως 17 ετών) και σε ενήλικες με διαβήτη τύπου 1. Παρόμοια με την ανθρώπινη ινσουλίνη NPH παρατηρήθηκε ελαφρώς υψηλότερη περιοχή πλάσματος κάτω από την καμπύλη (AUC) και Cmax στα παιδιά κατά 10% και 24% αντίστοιχα, σε σύγκριση με εφήβους και ενήλικες. Δεν υπήρχε διαφορά στη φαρμακοκινητική μεταξύ εφήβων και ενηλίκων.
Γηριατρική - Σε μια κλινική δοκιμή που διερευνά τις διαφορές στη φαρμακοκινητική μιας μόνο υποδόριας δόσης Levemir σε νέους (25 έως 35 ετών) ετών) έναντι των ηλικιωμένων (≥ 68 ετών) υγιή άτομα, υψηλότερα επίπεδα AUC ινσουλίνης (έως 35%) βρέθηκαν σε ηλικιωμένους ασθενείς λόγω μειωμένης εκτελωνισμός. Όπως και με άλλα σκευάσματα ινσουλίνης, το Levemir θα πρέπει πάντα να τιτλοδοτείται σύμφωνα με τις επιμέρους απαιτήσεις.
Φύλο - Σε ελεγχόμενες κλινικές μελέτες, δεν παρατηρείται κλινικά σημαντική διαφορά μεταξύ φύλων στις φαρμακοκινητικές παραμέτρους που βασίζονται σε αναλύσεις υποομάδων.
Φυλή - Σε δύο δοκιμές σε υγιή ιαπωνικά και καυκάσια άτομα, δεν παρατηρήθηκαν κλινικά σημαντικές διαφορές στις φαρμακοκινητικές παραμέτρους. Η φαρμακοκινητική και η φαρμακοδυναμική του Levemir διερευνήθηκαν σε μια δοκιμή σφιγκτήρα συγκρίνοντας τους ασθενείς με διαβήτη τύπου 2 με καυκάσια, αφροαμερικανική και λατινική προέλευση. Οι σχέσεις δόσης-απόκρισης ήταν συγκρίσιμες για το Levemir σε αυτούς τους τρεις πληθυσμούς.
Νεφρική δυσλειτουργία - Τα άτομα με νεφρική δυσλειτουργία δεν παρουσίασαν διαφορά στις φαρμακοκινητικές παραμέτρους σε σύγκριση με τους υγιείς εθελοντές. Ωστόσο, οι εκθέσεις από τη βιβλιογραφία έχουν δείξει ότι η κάθαρση της ανθρώπινης ινσουλίνης μειώνεται στους ασθενείς με νεφρική δυσλειτουργία. Η προσεκτική παρακολούθηση της γλυκόζης και η προσαρμογή της δόσης της ινσουλίνης, συμπεριλαμβανομένου του Levemir, μπορεί να είναι απαραίτητες σε ασθενείς με νεφρική δυσλειτουργία (βλ. ΠΡΟΦΥΛΑΞΕΙΣ, Νεφρική δυσλειτουργία).
Ηπατική δυσλειτουργία - Τα άτομα με σοβαρή ηπατική δυσλειτουργία, χωρίς διαβήτη, παρατηρήθηκαν να έχουν χαμηλότερες AUC σε σύγκριση με τους υγιείς εθελοντές. Η προσεκτική παρακολούθηση της γλυκόζης και η προσαρμογή της δόσης της ινσουλίνης, συμπεριλαμβανομένου του Levemir, μπορεί να είναι απαραίτητες σε ασθενείς με ηπατική δυσλειτουργία (βλ. ΠΡΟΦΥΛΑΞΕΙΣ, Η ηπατική βλάβη).
Εγκυμοσύνη - Η επίδραση της εγκυμοσύνης στη φαρμακοκινητική και τη φαρμακοδυναμική του Levemir δεν έχει μελετηθεί (βλ. ΠΡΟΦΥΛΑΞΕΙΣ, Εγκυμοσύνη).
Κάπνισμα - Η επίδραση του καπνίσματος στη φαρμακοκινητική και τη φαρμακοδυναμική του Levemir δεν έχει μελετηθεί.
μπλουζα
Κλινικές μελέτες
Η αποτελεσματικότητα και η ασφάλεια του Levemir χορηγούμενες μία φορά την ημέρα πριν από το βραδινό ύπνο ή δύο φορές την ημέρα (πριν από το πρωινό και πριν από το βραδινό, πριν από το πρωινό και με το βραδινό γεύμα ή σε διαστήματα 12 ωρών) συγκρίθηκε με αυτή της ΝΡΗ ανθρώπινης ινσουλίνης μία φορά ημερησίως ή δύο φορές ημερησίως ή μία φορά την ημέρα ινσουλίνης glargine σε μη τυφλές, τυχαιοποιημένες, παράλληλες μελέτες 6004 ασθενών με διαβήτη (3724 με τύπο 1 και 2280 με τύπο 2). Γενικά, οι ασθενείς που έλαβαν θεραπεία με Levemir πέτυχαν επίπεδα γλυκαιμικού ελέγχου παρόμοια με εκείνα που έλαβαν θεραπεία με ΝΡΗ ανθρώπινη ινσουλίνη ή ινσουλίνη glargine, όπως μετρήθηκε με γλυκοζυλιωμένη αιμοσφαιρίνη (HbA1c).
Διαβήτης τύπου 1 - Ενήλικας
Σε μία μη τυφλή κλινική μελέτη (Μελέτη Α, η = 409), οι ενήλικες ασθενείς με διαβήτη τύπου 1 τυχαιοποιήθηκαν θεραπεία με Levemir σε διαστήματα 12 ωρών, πρωί και ύπνο Levemir ή με πρωινό ανθρώπινης ινσουλίνης NPH και ώρα ύπνου. Η ινσουλίνη aspart χορηγήθηκε επίσης πριν από κάθε γεύμα. Στις 16 εβδομάδες θεραπείας, οι συνδυασμένοι ασθενείς που έλαβαν θεραπεία με Levemir είχαν παρόμοιες μειώσεις της γλυκόζης στο πλάσμα (HGA1c) και της γλυκόζης στο πλάσμα νηστείας σε ασθενείς που έλαβαν ΝΡΗ (Πίνακας 1). Οι διαφορές στον συγχρονισμό της χορήγησης του Levemir (ή της εύκαμπτης δοσολογίας) δεν είχαν καμία επίδραση στην HbA1c, FPG, το σωματικό βάρος ή στον κίνδυνο εμφάνισης υπογλυκαιμικών επεισοδίων.
Ο συνολικός γλυκαιμικός έλεγχος που επιτεύχθηκε με το Levemir συγκρίθηκε με εκείνον που επιτεύχθηκε με την ινσουλίνη glargine σε μια τυχαιοποιημένη, μη τυφλή κλινική μελέτη (μελέτη Β, n = 320) στους οποίους οι ασθενείς με διαβήτη τύπου 1 υποβλήθηκαν σε θεραπεία για 26 εβδομάδες είτε με ινσουλίνη Levemir δύο φορές ημερησίως (πρωί και ύπνο) είτε μία φορά την ημέρα glargine. Η ινσουλίνη aspart χορηγήθηκε πριν από κάθε γεύμα. Οι ασθενείς που έλαβαν Levemir παρουσίασαν μείωση της HbA1c παρόμοια με αυτή των ασθενών που έλαβαν ινσουλίνη glargine.
Σε μια τυχαιοποιημένη, ελεγχόμενη κλινική μελέτη (Μελέτη C, n = 749), ασθενείς με διαβήτη τύπου 1 έλαβαν θεραπεία μία φορά την ημέρα (πριν την κατάκλιση) Levemir ή NPH ανθρώπινη ινσουλίνη, και σε συνδυασμό με ανθρώπινη διαλυτή ινσουλίνη πριν από κάθε γεύμα 6 μήνες. Η ανθρώπινη ινσουλίνη Levemir και NPH είχε παρόμοιο αποτέλεσμα στην HbA1c.
Πίνακας 1: Αποτελεσματικότητα και Δοσολογία Ινσουλίνης στον Σακχαρώδη Διαβήτη Τύπου 1 - Ενήλικες
| Μελέτη A | ||
| Διάρκεια θεραπείας | 16 εβδομάδες | |
| Θεραπεία σε συνδυασμό με | NovoLog® (ασπαρτική ινσουλίνη) | |
| Levemir | NPH | |
| Αριθμός υποκειμένων θεραπείας | 276 | 133 |
| HbA1c (%) | ||
| Βασική γραμμή | 8.64 | 8.51 |
| Τέλος της μελέτης προσαρμοσμένη μέση | 7.76 | 7.94 |
| Μέση αλλαγή από τη γραμμή βάσης | -0.82 | -0.60 |
| Γλυκόζη πλάσματος νηστείας (mg / dL) | ||
| Τέλος της μελέτης προσαρμοσμένη μέση | 168 | 202 |
| Μέση αλλαγή από τη γραμμή βάσης | -42.48 | -10.80 |
| Ημερήσια βασική δόση ινσουλίνης (U / kg) | ||
| Έχει σημασία το Prestudy | 0.36 | 0.39 |
| Τέλος της μελέτης σημαίνει | 0.49 | 0.45 |
| Ημερήσια δόση ινσουλίνης Bolus (U / kg) | ||
| Έχει σημασία το Prestudy | 0.40 | 0.40 |
| Τέλος της μελέτης σημαίνει | 0.38 | 0.38 |
Οι αρχικές τιμές συμπεριελήφθησαν ως συντεταγμένες σε ανάλυση ANCOVA. |
Διαβήτης τύπου 1 - Παιδιατρικό
Σε μια μη τυφλή, τυχαιοποιημένη, ελεγχόμενη κλινική μελέτη (μελέτη D, n = 347), οι παιδιατρικοί ασθενείς (ηλικίας 6 έως 17 ετών) με διαβήτη τύπου 1 υποβλήθηκαν σε θεραπεία για 26 εβδομάδες με δοσολογία βασικής δόσης ινσουλίνης. Η Levemir και η ΝΡΗ ανθρώπινη ινσουλίνη χορηγήθηκαν μία φορά ή δύο φορές την ημέρα (πριν από την κατάκλιση ή την πρωινή και την ώρα του ύπνου) σύμφωνα με το προτασιακό σχήμα δόσης. Η Bolus ινσουλίνη ασπαρτική χορηγήθηκε πριν από κάθε γεύμα. Οι ασθενείς που έλαβαν Levemir είχαν μια μείωση στην HbA1c παρόμοια με εκείνη της ανθρώπινης ινσουλίνης NPH.
Πίνακας 2: Αποτελεσματικότητα και δοσολογία ινσουλίνης στον σακχαρώδη διαβήτη τύπου 1 - παιδιατρικό
| Μελέτη D | ||
| Διάρκεια θεραπείας | 26 εβδομάδες | |
| Θεραπεία σε συνδυασμό με | NovoLog® (ασπαρτική ινσουλίνη) | |
| Levemir | NPH | |
| Αριθμός υποκειμένων θεραπείας | 232 | 115 |
| HbA1c (%) | ||
| Βασική γραμμή | 8.75 | 8.77 |
| Τέλος της μελέτης προσαρμοσμένη μέση | 8.02 | 7.93 |
| Μέση αλλαγή από τη γραμμή βάσης | -0.72 | -0.80 |
| Γλυκόζη πλάσματος νηστείας (mg / dL) | ||
| Τέλος της μελέτης προσαρμοσμένη μέση | 151.92 | 172.44 |
| Μέση αλλαγή από τη γραμμή βάσης | -45.00 | -19.98 |
| Ημερήσια βασική δόση ινσουλίνης (U / kg) | ||
| Έχει σημασία το Prestudy | 0.48 | 0.49 |
| Τέλος της μελέτης σημαίνει | 0.67 | 0.64 |
| Ημερήσια δόση ινσουλίνης Bolus (U / kg) | ||
| Έχει σημασία το Prestudy | 0.52 | 0.47 |
| Τέλος της μελέτης σημαίνει | 0.52 | 0.51 |
Διαβήτης τύπου 2 - Ενήλικας
Σε μια μη τυφλή τυχαιοποιημένη κλινική μελέτη 24 εβδομάδων (Μελέτη Ε, η = 476), το Levemir που χορηγήθηκε δύο φορές την ημέρα (πριν από το πρωινό και το βράδυ) συγκρίθηκε με παρόμοιο σχήμα ΝΡΗ ανθρώπινη ινσουλίνη ως μέρος ενός σχήματος συνδυαστικής θεραπείας με έναν ή δύο από τους ακόλουθους από του στόματος αντιδιαβητικούς παράγοντες (μετφορμίνη, εκκριταγωγός ινσουλίνης ή ϋ-γλυκοσιδάση ανασταλτικός παράγοντας). Το Levemir και το NPH μείωσαν παρομοίως την HbA1c από την αρχική τιμή (Πίνακας 3).
Πίνακας 3: Αποτελεσματικότητα και Δοσολογία Ινσουλίνης στον Σακχαρώδη Διαβήτη Τύπου 2
| Μελέτη Ε | ||
| Διάρκεια θεραπείας | 24 εβδομάδες | |
| Θεραπεία σε συνδυασμό με | OAD | |
| Levemir | NPH | |
| Αριθμός υποκειμένων θεραπείας | 237 | 239 |
| HbA1c (%) | ||
| Βασική γραμμή | 8.61 | 8.51 |
| Τέλος της μελέτης προσαρμοσμένη μέση | 6.58 | 6.46 |
| Μέση αλλαγή από τη γραμμή βάσης | -1.84 | -1.90 |
| Ποσοστό επίτευξης της HbA1γ ≤ 7% | 70% | 74% |
| Γλυκόζη πλάσματος νηστείας (mg / dL) | ||
| Τέλος της μελέτης προσαρμοσμένη μέση | 119.16 | 113.40 |
| Μέση αλλαγή από τη γραμμή βάσης | -75.96 | -74.34 |
| Ημερήσια δόση ινσουλίνης (U / kg) | ||
| Τέλος της μελέτης σημαίνει | 0.77 | 0.52 |
Σε μια 22-εβδομάδα, μη τυφλή, τυχαιοποιημένη κλινική μελέτη (μελέτη F, n = 395) σε ενήλικες με διαβήτη τύπου 2, η ανθρώπινη ινσουλίνη Levemir και NPH χορηγήθηκε μία φορά ή δύο φορές ημερησίως ως τμήμα βασικής δόσης. Όπως μετρήθηκε με HbA1c ή FPG, το Levemir είχε αποτελεσματικότητα παρόμοια με την ανθρώπινη ινσουλίνη NPH.
μπλουζα
Ενδείξεις και χρήση
Το Levemir ενδείκνυται για υποδόρια χορήγηση μία ή δύο φορές την ημέρα για τη θεραπεία ενηλίκων και παιδιατρικών ασθενών τύπου 1 σακχαρώδη διαβήτη ή ενήλικες ασθενείς με σακχαρώδη διαβήτη τύπου 2 που χρειάζονται βασική (μακράς δράσης) ινσουλίνη για τον έλεγχο της υπεργλυκαιμία.
μπλουζα
Αντενδείξεις
Το Levemir αντενδείκνυται σε ασθενείς που παρουσιάζουν υπερευαισθησία στην ινσουλίνη detemir ή σε κάποιο από τα έκδοχα του.
μπλουζα
Προειδοποιήσεις
Η υπογλυκαιμία είναι η πιο συχνή ανεπιθύμητη ενέργεια της ινσουλινοθεραπείας, συμπεριλαμβανομένου του Levemir. Όπως συμβαίνει με όλες τις ινσουλίνες, ο συγχρονισμός της υπογλυκαιμίας μπορεί να διαφέρει μεταξύ των διαφόρων συνθέσεων ινσουλίνης.
Η παρακολούθηση της γλυκόζης συνιστάται για όλους τους ασθενείς με διαβήτη.
Το Levemir δεν πρέπει να χρησιμοποιείται σε αντλίες έγχυσης ινσουλίνης.
Οποιαδήποτε αλλαγή της δόσης ινσουλίνης πρέπει να γίνεται προσεκτικά και μόνο υπό ιατρική παρακολούθηση. Μεταβολές στην ισχύ ινσουλίνης, χρόνος δοσολογίας, κατασκευαστής, τύπος (π.χ. τακτική, ΝΡΗ ή ανάλογα ινσουλίνης), είδος (ζώο, άνθρωπος) ή μέθοδο παρασκευής (rDNA έναντι ινσουλίνης ζωικής προέλευσης) μπορεί να έχει ως αποτέλεσμα την ανάγκη αλλαγής σε δοσολογία.
Μπορεί να χρειαστεί προσαρμογή της ταυτόχρονης αντιδιαβητικής θεραπείας από του στόματος.
μπλουζα
Προφυλάξεις
Γενικός
Η ανεπαρκής δοσολογία ή η διακοπή της θεραπείας μπορεί να οδηγήσει σε υπεργλυκαιμία και, σε ασθενείς με διαβήτη τύπου 1, διαβητική κετοξέωση. Τα πρώτα συμπτώματα της υπεργλυκαιμίας συνήθως εμφανίζονται σταδιακά σε μια περίοδο ωρών ή ημερών. Περιλαμβάνουν ναυτία, έμετο, υπνηλία, ξεπλυμένο ξηρό δέρμα, ξηροστομία, αυξημένη ούρηση, δίψα και απώλεια όρεξης καθώς και αναπνοή ακετόνης. Τα ανεπεξέργαστα υπεργλυκαιμικά συμβάντα είναι δυνητικά θανατηφόρα.
Το Levemir δεν προορίζεται για ενδοφλέβια ή ενδομυϊκή χορήγηση. Η παρατεταμένη διάρκεια της δράσης της ινσουλίνης detemir εξαρτάται από την ένεση στον υποδόριο ιστό. Η ενδοφλέβια χορήγηση της συνήθους υποδόριας δόσης μπορεί να οδηγήσει σε σοβαρή υπογλυκαιμία. Η απορρόφηση μετά από ενδομυϊκή χορήγηση είναι ταχύτερη και εκτενέστερη από την απορρόφηση μετά από υποδόρια χορήγηση.
Το Levemir δεν πρέπει να αραιώνεται ή να αναμειγνύεται με άλλα σκευάσματα ινσουλίνης (βλ ΠΡΟΦΥΛΑΞΕΙΣ, Ανάμιξη ινσουλινών).
Η ινσουλίνη μπορεί να προκαλέσει κατακράτηση νατρίου και οίδημα, ιδιαίτερα εάν βελτιωθεί προηγουμένως ο μεταβολικός έλεγχος με εντατική θεραπεία ινσουλίνης.
Η λιποδυστροφία και η υπερευαισθησία αποτελούν πιθανές κλινικές ανεπιθύμητες ενέργειες που σχετίζονται με τη χρήση όλων των ινσουλινών.
Όπως συμβαίνει με όλα τα σκευάσματα ινσουλίνης, η χρονική πορεία της δράσης του Levemir μπορεί να ποικίλει σε διαφορετικά άτομα ή σε διαφορετικές χρονικές στιγμές στο ίδιο άτομο και εξαρτάται από το σημείο της ένεσης, την παροχή αίματος, τη θερμοκρασία και τη σωματική δραστηριότητα.
Η προσαρμογή της δοσολογίας οποιασδήποτε ινσουλίνης μπορεί να είναι απαραίτητη εάν οι ασθενείς αλλάξουν τη σωματική τους δραστηριότητα ή το συνηθισμένο σχέδιο γεύματος τους.
Υπογλυκαιμία
Όπως συμβαίνει με όλα τα σκευάσματα ινσουλίνης, οι υπογλυκαιμικές αντιδράσεις μπορεί να σχετίζονται με τη χορήγηση του Levemir. Η υπογλυκαιμία είναι η πιο συχνή ανεπιθύμητη ενέργεια των ινσουλινών. Τα πρόδρομα προειδοποιητικά συμπτώματα της υπογλυκαιμίας μπορεί να είναι διαφορετικά ή λιγότερο έντονα υπό ορισμένες συνθήκες, όπως η μεγάλη τη διάρκεια του διαβήτη, τη νόσο του διαβητικού νεύρου, τη χρήση φαρμάκων όπως οι β-αναστολείς ή τον ενισχυμένο έλεγχο του διαβήτη (βλέπω ΠΡΟΦΥΛΑΞΕΙΣ, Αλληλεπιδράσεις με άλλα φάρμακα). Τέτοιες καταστάσεις μπορεί να οδηγήσουν σε σοβαρή υπογλυκαιμία (και, ενδεχομένως, απώλεια συνείδησης) πριν από την ευαισθητοποίηση των ασθενών για υπογλυκαιμία.
Ο χρόνος εμφάνισης της υπογλυκαιμίας εξαρτάται από το προφίλ δράσης των χρησιμοποιούμενων ινσουλινών και κατά συνέπεια μπορεί να αλλάξει όταν αλλάζει η θεραπευτική αγωγή ή η χρονική στιγμή της δοσολογίας. Σε ασθενείς που μεταβαίνουν από άλλα ενδιάμεσα ή μακροχρόνια παρασκευάσματα ινσουλίνης σε Levemir μία φορά ή δύο φορές ημερησίως, οι δόσεις μπορούν να συνταγογραφούνται σε μονάδα ανά μονάδα. Ωστόσο, όπως και σε όλα τα σκευάσματα ινσουλίνης, η δόση και ο χρόνος χορήγησης μπορεί να χρειαστεί να προσαρμοστούν για να μειωθεί ο κίνδυνος υπογλυκαιμίας (βλ. ΔΟΣΟΛΟΓΙΑ ΚΑΙ ΧΟΡΗΓΗΣΗ, Μετάβαση στο Levemir).
Νεφρική δυσλειτουργία
Όπως και με άλλες ινσουλίνες, οι απαιτήσεις για το Levemir ενδέχεται να πρέπει να προσαρμοστούν σε ασθενείς με νεφρική ανεπάρκεια (βλ ΚΛΙΝΙΚΗ ΦΑΡΜΑΚΟΛΟΓΙΑ, Φαρμακοκινητική).
Ηπατική ανεπάρκεια
Όπως και με άλλες ινσουλίνες, οι απαιτήσεις για το Levemir μπορεί να χρειαστεί να προσαρμοστούν σε ασθενείς με ηπατική δυσλειτουργία (βλ ΚΛΙΝΙΚΗ ΦΑΡΜΑΚΟΛΟΓΙΑ, Φαρμακοκινητική).
Χώρος έγχυσης και αλλεργικές αντιδράσεις
Όπως και με οποιαδήποτε θεραπεία με ινσουλίνη, μπορεί να εμφανιστεί λιποδυστροφία στο σημείο της ένεσης και να καθυστερήσει την απορρόφηση της ινσουλίνης. Άλλες αντιδράσεις της θέσης ένεσης με θεραπεία ινσουλίνης μπορεί να περιλαμβάνουν ερυθρότητα, πόνο, κνησμό, κνίδωση, οίδημα και φλεγμονή. Η συνεχής περιστροφή του σημείου της ένεσης μέσα σε μια δεδομένη περιοχή μπορεί να βοηθήσει στη μείωση ή την πρόληψη αυτών των αντιδράσεων. Οι αντιδράσεις συνήθως λύνονται σε λίγες μέρες έως μερικές εβδομάδες. Σε σπάνιες περιπτώσεις, οι αντιδράσεις στο σημείο της ένεσης μπορεί να απαιτούν διακοπή του Levemir.
Σε ορισμένες περιπτώσεις, αυτές οι αντιδράσεις μπορεί να σχετίζονται με άλλους παράγοντες εκτός από την ινσουλίνη, όπως ερεθιστικά μέσα σε ένα μέσο καθαρισμού του δέρματος ή με κακή τεχνική ένεσης.
Συστηματική αλλεργία: Η γενικευμένη αλλεργία στην ινσουλίνη, η οποία είναι λιγότερο συχνή αλλά δυνητικά πιο σοβαρή, μπορεί να προκαλέσει εξάνθημα (συμπεριλαμβανομένου του κνησμού) σε ολόκληρο το σώμα, δυσκολία στην αναπνοή, συριγμό, μείωση της αρτηριακής πίεσης, γρήγορος παλμός ή ιδρώνοντας. Οι σοβαρές περιπτώσεις γενικευμένης αλλεργίας, συμπεριλαμβανομένης της αναφυλακτικής αντίδρασης, μπορεί να είναι απειλητικές για τη ζωή.
Συνυπάρχουσες συνθήκες
Οι ανάγκες σε ινσουλίνη μπορεί να μεταβάλλονται κατά τη διάρκεια διαταραγμένων συνθηκών, όπως ασθένεια, συναισθηματικές διαταραχές ή άλλες καταπονήσεις.
Πληροφορίες για τους ασθενείς
Το Levemir πρέπει να χρησιμοποιείται μόνο εάν το διάλυμα είναι διαυγές και άχρωμο χωρίς ορατά σωματίδια (βλ ΔΟΣΟΛΟΓΙΑ ΚΑΙ ΧΟΡΗΓΗΣΗ, Προετοιμασία και χειρισμός). Οι ασθενείς θα πρέπει να ενημερώνονται για τους πιθανούς κινδύνους και τα πλεονεκτήματα της θεραπείας με Levemir, συμπεριλαμβανομένων των πιθανών ανεπιθύμητων ενεργειών. Πρέπει να παρέχεται στους ασθενείς η συνεχής εκπαίδευση και συμβουλές σχετικά με τις θεραπείες ινσουλίνης, την τεχνική ένεσης, τη διαχείριση του τρόπου ζωής, την τακτική παρακολούθηση της γλυκόζης, τον περιοδικό έλεγχο της γλυκοζυλιωμένης αιμοσφαιρίνης, την αναγνώριση και τη διαχείριση της υπο-και υπεργλυκαιμίας, την τήρηση του σχεδιασμού των γευμάτων, τις επιπλοκές της θεραπείας με ινσουλίνη, το χρονοδιάγραμμα της δοσολογίας, την οδηγία χρήσης των συσκευών ένεσης και τη σωστή αποθήκευση ινσουλίνη. Οι ασθενείς θα πρέπει να ενημερώνονται ότι απαιτούνται συχνά μετρήσεις γλυκόζης αίματος που πραγματοποιούνται από τον ασθενή για να επιτευχθεί αποτελεσματικός γλυκαιμικός έλεγχος για την αποφυγή τόσο της υπεργλυκαιμίας όσο και της υπογλυκαιμίας. Οι ασθενείς πρέπει να ενημερώνονται σχετικά με το χειρισμό ειδικών καταστάσεων, όπως διαταραχές (ασθένεια, άγχος ή συναισθηματική κατάσταση διαταραχές), ανεπαρκή ή παραλειφθείσα δόση ινσουλίνης, ακούσια χορήγηση αυξημένης δόσης ινσουλίνης, ανεπαρκής λήψη τροφής ή παραλείψει τα γεύματα. Ανατρέξτε στους ασθενείς στην εγκύκλιο Levemir "Πληροφορίες ασθενούς" για περισσότερες πληροφορίες.
Όπως συμβαίνει με όλους τους ασθενείς που έχουν διαβήτη, η ικανότητα συγκέντρωσης και / ή αντίδρασης μπορεί να επηρεαστεί ως αποτέλεσμα της υπογλυκαιμίας ή της υπεργλυκαιμίας.
Οι ασθενείς με διαβήτη θα πρέπει να ενημερώνονται για να ενημερώσουν τον επαγγελματία υγείας τους εάν είναι έγκυοι ή σκέφτονται την εγκυμοσύνη (βλ ΠΡΟΦΥΛΑΞΕΙΣ, Εγκυμοσύνη).
Εργαστηριακές δοκιμές
Όπως με όλες τις θεραπείες ινσουλίνης, η θεραπευτική ανταπόκριση στο Levemir πρέπει να παρακολουθείται με περιοδικές εξετάσεις γλυκόζης στο αίμα. Η περιοδική μέτρηση της HbA1c συνιστάται για την παρακολούθηση του μακροχρόνιου γλυκαιμικού ελέγχου.
Αλληλεπιδράσεις με άλλα φάρμακα
Ορισμένες ουσίες επηρεάζουν τον μεταβολισμό της γλυκόζης και μπορεί να απαιτούν προσαρμογή της δόσης ινσουλίνης και ιδιαίτερα στενή παρακολούθηση.
Τα παρακάτω είναι παραδείγματα ουσιών που μπορούν να μειώσουν την επίδραση της ινσουλίνης στη μείωση της γλυκόζης στο αίμα: κορτικοστεροειδή, δαναζόλη, διουρητικά, συμπαθητικομιμητικά μέσα (π.χ., επινεφρίνη, αλβουτερόλη, τερβουταλίνη), ισονιαζίδιο, παράγωγα φαινοθειαζίνης, σωματοτροπίνη, θυρεοειδείς ορμόνες, οιστρογόνα, προγεστογόνα (π.χ. αντισυλληπτικά).
Τα παρακάτω είναι παραδείγματα ουσιών που μπορούν να αυξήσουν την επίδραση της ινσουλίνης στη μείωση της γλυκόζης του αίματος και την ευαισθησία στην υπογλυκαιμία: από του στόματος αντιδιαβητική φάρμακα, αναστολείς ACE, δισοπυραμίδη, φιβράτες, φλουοξετίνη, αναστολείς ΜΑΟ, προποξυφαίνη, σαλικυλικά άλατα, ανάλογα σωματοστατίνης (π.χ. οκτρεοτίδιο) και σουλφοναμίδιο αντιβιοτικά.
Οι β-αναστολείς, η κλονιδίνη, τα άλατα λιθίου και η αλκοόλη μπορούν είτε να ενισχύσουν είτε να αποδυναμώσουν την επίδραση της ινσουλίνης στη μείωση της γλυκόζης στο αίμα. Η πενταμιδίνη μπορεί να προκαλέσει υπογλυκαιμία, η οποία μπορεί μερικές φορές να ακολουθείται από υπεργλυκαιμία. Επιπλέον, υπό την επήρεια συμπαθολυτικών φαρμακευτικών προϊόντων όπως οι βήτα-αναστολείς, η κλονιδίνη, η γουα-λεθιδίνη και η ρεσερπίνη, τα σημάδια της υπογλυκαιμίας μπορεί να μειωθούν ή να απουσιάζουν.
Τα αποτελέσματα των in-vitro και in-vivo μελετών σύνδεσης με πρωτεΐνες αποδεικνύουν ότι δεν υπάρχει κλινικά σχετική αλληλεπίδραση μεταξύ insulin detemir και λιπαρών οξέων ή άλλων πρωτεϊνικών δεσμευμένων φαρμάκων.
Μίξη ινσουλινών
Εάν το Levemir αναμειχθεί με άλλα σκευάσματα ινσουλίνης, το προφίλ δράσης ενός ή και των δύο μεμονωμένων συστατικών μπορεί να αλλάξει. Η ανάμειξη του Levemir με ινσουλίνη ασπαρτική, ένα ανάλογο ινσουλίνης ταχείας δράσης, οδήγησε σε περίπου 40% μείωση της AUC (0-2h) και Cmax για ινσουλίνη aspart σε σύγκριση με ξεχωριστές ενέσεις όταν η αναλογία ινσουλίνης aspart προς Levemir ήταν μικρότερη από 50%.
Το Levemir ΔΕΝ πρέπει να αναμιγνύεται ή να αραιώνεται με άλλα σκευάσματα ινσουλίνης.
Καρκινογένεση, Μεταλλαξογένεση, Βλάβη της Γονιμότητας
Δεν έχουν διεξαχθεί κανονικές 2ετές μελέτες καρκινογένεσης σε ζώα. Η ινσουλίνη detemir κατέδειξε αρνητικό για γονιδιοτοξικό δυναμικό στην in vitro μελέτη της ανάστροφης μετάλλαξης στην Ινδία βακτήρια, δοκιμασία εκτροπής χρωμοσώματος ανθρώπινου περιφερικού αίματος λεμφοκυττάρων και τον ίη νίνο ποντικό δοκιμή μικροπυρήνων.
Εγκυμοσύνη
Κατηγορία εγκυμοσύνης C
Τερατογόνες επιδράσεις
Σε μελέτη γονιμότητας και εμβρυονικής ανάπτυξης, η ινσουλίνη detemir χορηγήθηκε σε θηλυκούς αρουραίους πριν από το ζευγάρωμα, κατά τη διάρκεια του ζευγαρώματος και κατά τη διάρκεια της εγκυμοσύνης σε δόσεις έως 300 nmol / kg / ημέρα (3 φορές τη συνιστώμενη δόση για τον άνθρωπο, με βάση την περιοχή πλάσματος κάτω από την καμπύλη (AUC) αναλογία). Δόσεις των 150 και 300 nmol / kg / ημέρα παρήγαγαν αριθμούς νεογνών με σπλαχνικές ανωμαλίες. Δόσεις έως 900 nmol / kg / ημέρα (κατά προσέγγιση 135 φορές τη συνιστώμενη δόση ανθρώπινης δόσης με βάση την αναλογία AUC) χορηγήθηκαν σε κουνέλια κατά τη διάρκεια της οργανογένεσης. Έχουν παρατηρηθεί αυξήσεις στη συχνότητα εμφάνισης εμβρύων με ανωμαλίες της χοληδόχου κύστης, όπως μικρές, διχοτομημένες, διχαλωτές και λείπουν χοληδόχοι κύστεις σε δόση 900 nmol / kg / ημέρα. Οι μελέτες ανάπτυξης εμβρυοσωματικής ανάπτυξης επίμυων και κουνελιού που περιελάμβαναν ταυτόχρονες ομάδες ελέγχου ανθρώπινης ινσουλίνης έδειξε ότι η ινσουλίνη detemir και η ανθρώπινη ινσουλίνη είχαν παρόμοιες επιδράσεις όσον αφορά την εμβρυοτοξικότητα και τερατογένεση.
Οι θηλάζουσες μητέρες
Δεν είναι γνωστό εάν το Levemir εκκρίνεται σε σημαντικές ποσότητες στο ανθρώπινο γάλα. Για το λόγο αυτό, πρέπει να δίδεται προσοχή όταν το Levemir χορηγείται σε θηλάζουσα μητέρα. Οι ασθενείς με διαβήτη που θηλάζουν μπορεί να χρειαστούν προσαρμογές στη δόση ινσουλίνης, σχέδιο γεύματος ή και στα δύο.
Παιδιατρική χρήση
Σε μια ελεγχόμενη κλινική μελέτη, οι συγκεντρώσεις HbA1c και τα ποσοστά υπογλυκαιμίας ήταν παρόμοια μεταξύ των ασθενών που έλαβαν θεραπεία με Levemir και των ασθενών που υποβλήθηκαν σε θεραπεία με ανθρώπινη ινσουλίνη NPH.
Γηριακή χρήση
Από το συνολικό αριθμό ασθενών στις ενδιάμεσες και μακροπρόθεσμες κλινικές μελέτες του Levemir, 85 (μελέτες τύπου 1) και 363 (μελέτες τύπου 2) ήταν 65 ετών και άνω. Δεν παρατηρήθηκαν γενικές διαφορές όσον αφορά την ασφάλεια ή την αποτελεσματικότητα μεταξύ αυτών των ατόμων και των νεότερων ατόμων και έχει αναφερθεί και άλλη αναφερθείσα κλινική εμπειρία δεν εντοπίστηκαν διαφορές στις αντιδράσεις μεταξύ ηλικιωμένων και νεότερων ασθενών, αλλά δεν μπορεί να αποκλειστεί η μεγαλύτερη ευαισθησία ορισμένων ηλικιωμένων ατόμων. Σε ηλικιωμένους ασθενείς με διαβήτη, η αρχική δοσολογία, η αύξηση της δόσης και η δοσολογία συντήρησης πρέπει να είναι συντηρητικές για την αποφυγή υπογλυκαιμικών αντιδράσεων. Η υπογλυκαιμία μπορεί να είναι δύσκολο να αναγνωριστεί στους ηλικιωμένους.
μπλουζα
Ανεπιθύμητες ενέργειες
Τα ανεπιθύμητα συμβάντα που συνήθως σχετίζονται με τη θεραπεία με ανθρώπινη ινσουλίνη περιλαμβάνουν τα ακόλουθα:
Σώμα ως σύνολο: αλλεργικές αντιδράσεις (βλ ΠΡΟΦΥΛΑΞΕΙΣ, Αλλεργία).
Δέρμα και παρεμβολές: λιποδυστροφία, κνησμός, εξάνθημα. Ήπιες αντιδράσεις στο σημείο της ένεσης εμφανίστηκαν συχνότερα με το Levemir παρά με την ανθρώπινη ινσουλίνη NPH και συνήθως διέφεραν σε λίγες μέρες έως μερικές εβδομάδες (βλ. ΠΡΟΦΥΛΑΞΕΙΣ, Αλλεργία).
Αλλα:
Υπογλυκαιμία: (βλ ΠΡΟΕΙΔΟΠΟΙΗΣΕΙΣ και ΠΡΟΦΥΛΑΞΕΙΣ).
Σε δοκιμές διάρκειας έως και 6 μηνών σε ασθενείς με διαβήτη τύπου 1 και τύπου 2, η συχνότητα εμφάνισης σοβαρής υπογλυκαιμίας με Το Levemir ήταν συγκρίσιμο με το ποσοστό εμφάνισης με ΝΡΗ και, όπως αναμενόταν, υψηλότερο συνολικά σε ασθενείς με διαβήτη τύπου 1 (Πίνακας 2) 4).
Αύξηση βάρους:
Σε μελέτες διάρκειας έως και 6 μηνών σε ασθενείς με διαβήτη τύπου 1 και τύπου 2, το Levemir συσχετίστηκε με κάπως μικρότερη αύξηση βάρους από το NPH (Πίνακας 4). Το εάν οι παρατηρηθείσες αυτές διαφορές αντιπροσωπεύουν αληθινές διαφορές στις επιδράσεις του Levemir και της ινσουλίνης NPH δεν είναι γνωστή, δεδομένου ότι αυτές οι δοκιμές δεν ήταν τυφλές και η τα πρωτόκολλα (π.χ. οδηγίες διατροφής και άσκησης και παρακολούθηση) δεν είχαν συγκεκριμένο στόχο να διερευνήσουν υποθέσεις που σχετίζονται με τις επιδράσεις βάρους των θεραπειών σε συγκριση. Η κλινική σημασία των παρατηρούμενων διαφορών δεν έχει τεκμηριωθεί.
Πίνακας 4: Πληροφορίες για την ασφάλεια στις κλινικές μελέτες *
| ||||||
| Βάρος (kg) | Υπογλυκαιμία (γεγονότα / θέμα / μήνα) | |||||
| Θεραπευτική αγωγή | # θέματα | Βασική γραμμή | Τέλος της θεραπείας | Μείζων†| Ανήλικοςντο | |
| Τύπος 1 | ||||||
| Μελέτη A | Levemir | Ν = 276 | 75.0 | 75.1 | 0.045 | 2.184 |
| NPH | Ν = 133 | 75.7 | 76.4 | 0.035 | 3.063 | |
| Μελέτη Γ | Levemir | Ν = 492 | 76.5 | 76.3 | 0.029 | 2.397 |
| NPH | Ν = 257 | 76.1 | 76.5 | 0.027 | 2.564 | |
| Μελέτη D Παιδιατρική | Levemir | Ν = 232 | N / A | N / A | 0.076 | 2.677 |
| NPH | Ν = 115 | N / A | N / A | 0.083 | 3.203 | |
| Τύπος 2 | ||||||
| Μελέτη Ε | Levemir | Ν = 237 | 82.7 | 83.7 | 0.001 | 0.306 |
| NPH | Ν = 239 | 82.4 | 85.2 | 0.006 | 0.595 | |
| Μελέτη F | Levemir | Ν = 195 | 81.8 | 82.3 | 0.003 | 0.193 |
| NPH | Ν = 200 | 79.6 | 80.9 | 0.006 | 0.235 |
μπλουζα
Υπερδοσολογία
Η υπογλυκαιμία μπορεί να συμβεί ως αποτέλεσμα της περίσσειας ινσουλίνης σε σχέση με την πρόσληψη τροφής, την ενεργειακή δαπάνη ή και τα δύο. Τα ήπια επεισόδια υπογλυκαιμίας συνήθως μπορούν να αντιμετωπιστούν με στοματική γλυκόζη. Μπορεί να χρειαστούν προσαρμογές στη δοσολογία του φαρμάκου, στα σχέδια γεύματος ή στην άσκηση. Τα σοβαρότερα επεισόδια με κώμα, κρίση ή νευρολογική ανεπάρκεια μπορούν να αντιμετωπιστούν με ενδομυϊκή / υποδόρια γλυκαγόνη ή με συμπυκνωμένη ενδοφλέβια γλυκόζη. Μετά από προφανή κλινική ανάκαμψη από την υπογλυκαιμία, η συνεχής παρακολούθηση και η πρόσληψη πρόσθετων υδατανθράκων μπορεί να είναι απαραίτητα για να αποφευχθεί η επανεμφάνιση υπογλυκαιμίας.
μπλουζα
Δοσολογία και χορήγηση
Το Levemir μπορεί να χορηγηθεί μία φορά ή δύο φορές την ημέρα. Η δόση του Levemir θα πρέπει να προσαρμόζεται σύμφωνα με τις μετρήσεις της γλυκόζης του αίματος. Η δοσολογία του Levemir πρέπει να εξατομικεύεται με βάση τις συμβουλές του γιατρού, σύμφωνα με τις ανάγκες του ασθενούς.
- Για τους ασθενείς που λαμβάνουν Levemir άπαξ ημερησίως, η δόση θα πρέπει να χορηγείται με το βραδινό γεύμα ή τον ύπνο.
- Για ασθενείς που χρειάζονται δόση δύο φορές ημερησίως για αποτελεσματικό έλεγχο της γλυκόζης στο αίμα, η βραδινή δόση μπορεί να χορηγηθεί είτε με το βραδινό γεύμα, κατά την ώρα του ύπνου είτε 12 ώρες μετά την πρωινή δόση.
Το Levemir πρέπει να χορηγείται με υποδόρια ένεση στον μηρό, στον κοιλιακό τοίχο ή στον άνω βραχίονα. Οι θέσεις έγχυσης πρέπει να περιστρέφονται εντός της ίδιας περιοχής. Όπως με όλες τις ινσουλίνες, η διάρκεια της δράσης ποικίλλει ανάλογα με τη δόση, το σημείο της ένεσης, τη ροή του αίματος, τη θερμοκρασία και το επίπεδο φυσικής δραστηριότητας.
Προσδιορισμός δόσης για το Levemir
- Για ασθενείς με σακχαρώδη διαβήτη τύπου 1 ή τύπου 2 σε βασική θεραπεία με bolus, η αλλαγή της βασικής ινσουλίνης στο Levemir μπορεί να γίνει με βάση τη μονάδα σε μονάδα. Η δόση του Levemir θα πρέπει στη συνέχεια να προσαρμόζεται για να επιτευχθούν οι γλυκαιμικοί στόχοι. Σε ορισμένους ασθενείς με διαβήτη τύπου 2, μπορεί να απαιτηθεί μεγαλύτερη δόση Levemir από την ινσουλίνη NPH. Σε μια κλινική μελέτη, η μέση δόση στο τέλος της θεραπείας ήταν 0,77 U / kg για το Levemir και 0,52 IU / kg για την ανθρώπινη ινσουλίνη NPH (βλ. Πίνακας 3).
- Για τους ασθενείς που λαμβάνουν μόνο βασική ινσουλίνη, η αλλαγή της βασικής ινσουλίνης στο Levemir μπορεί να γίνει σε μονάδα ανά μονάδα.
- Για τους ασθενείς με ινσουλίνη που πάσχουν από διαβήτη τύπου 2 οι οποίοι δεν ελέγχονται επαρκώς από τα από του στόματος αντιδιαβητικά φάρμακα, το Levemir πρέπει να ξεκινήσει σε δόση από 0,1 έως 0,2 U / kg μία φορά την ημέρα το βράδυ ή 10 μονάδες μία ή δύο φορές ημερησίως και η δόση ρυθμίζεται για να επιτευχθεί γλυκαιμική στόχων.
- Όπως συμβαίνει με όλες τις ινσουλίνες, συνιστάται στενή παρακολούθηση γλυκόζης κατά τη διάρκεια της μετάβασης και στις πρώτες εβδομάδες μετά. Η δόση και ο συγχρονισμός των ταυτόχρονα ινσουλίνης βραχείας δράσης ή άλλης ταυτόχρονης αντιδιαβητικής θεραπείας μπορεί να χρειαστεί να προσαρμοστούν.
Προετοιμασία και χειρισμός
Το Levemir θα πρέπει να επιθεωρείται οπτικά πριν από τη χορήγηση και θα πρέπει να χρησιμοποιείται μόνο εάν το διάλυμα είναι διαυγές και άχρωμο.
Το Levemir δεν πρέπει να αναμειγνύεται ή να αραιώνεται με άλλα σκευάσματα ινσουλίνης.
Μετά από κάθε ένεση, οι ασθενείς πρέπει να αφαιρέσουν τη βελόνα χωρίς αναστροφή και να την απορρίψουν σε ένα ανθεκτικό σε διάτρηση δοχείο. Οι χρησιμοποιημένες σύριγγες, βελόνες ή βελόνες πρέπει να τοποθετούνται σε δοχεία "αιχμηρών αντικειμένων" (όπως κόκκινος βιολογικός κίνδυνος δοχεία), σκληρούς πλαστικούς περιέκτες (όπως μπουκάλια απορρυπαντικών) ή μεταλλικά δοχεία (όπως ένα κενό δοχείο) καφέ). Αυτά τα δοχεία θα πρέπει να σφραγίζονται και να απορρίπτονται σωστά.
μπλουζα
Πώς παρέχεται
Το Levemir διατίθεται στα ακόλουθα μεγέθη συσκευασίας: κάθε παρουσίαση που περιέχει 100 μονάδες ινσουλίνης detemir ανά mL (U-100).
| Φιαλίδιο των 10 mL | NDC 0169-3687-12 |
| 3 mL PenFill® φυσίγγια * | NDC 0169-3305-11 |
| 3 mL InnoLet® | NDC 0169-2312-11 |
| 3 mL FlexPen® | NDC 0169-6439-10 |
* Τα φυσίγγια Levemir PenFill® προορίζονται για χρήση με συσκευές χορήγησης ινσουλίνης Novo Nordisk 3 mL PenFill® και βελόνες NovoFine®.
Τελευταία ενημέρωση 05/2007
Levemir, ινσουλίνη detemir (προέλευση rDNA), πληροφορίες για τον ασθενή (στην απλή αγγλική γλώσσα)
Λεπτομερείς πληροφορίες για σημεία, συμπτώματα, αιτίες, θεραπείες διαβήτη
Οι πληροφορίες σε αυτή τη μονογραφία δεν προορίζονται να καλύψουν όλες τις πιθανές χρήσεις, οδηγίες, προφυλάξεις, αλληλεπιδράσεις φαρμάκων ή ανεπιθύμητες ενέργειες. Αυτές οι πληροφορίες είναι γενικευμένες και δεν προορίζονται ως συγκεκριμένες ιατρικές συμβουλές. Εάν έχετε απορίες σχετικά με τα φάρμακα που παίρνετε ή θέλετε περισσότερες πληροφορίες, επικοινωνήστε με το γιατρό σας, το φαρμακοποιό ή τη νοσοκόμα σας.
πίσω στο: Περιηγηθείτε σε όλα τα φάρμακα για τον διαβήτη



